आप विलयनों से परिचित हैं। इनकी हमारे जीवन में महत्वपूर्ण भूमिका है। दूध,
मक्खन, पनीर, क्रीम, रंगीन रत्न, बूट पॉलिश, रबर, स्याही आदि अनेक पदार्थ हमारे जीवन
में महत्वपूर्ण भूमिका निभाते हैं। वे भी एक प्रकार के विलयन है। उन्हें कोलाइडी विलयन
कहते है।’कोला’ का अर्थ है सरेस और ‘आइड’ का अर्थ समान है ।
अर्थात् कोलाइड का अर्थ है - सरेस के समान। पानी में शर्करा के विलयन में
अथवा पानी में नमक के विलयन में विघमान कणों की अपेक्षा कोलाइडी विलयन में
विघमान कणों का आमाप बड़ा होता है। इस पाठ में आप कोलाइडी विलयनों को बनाने
की विधियाँ, उनके गुणधर्म और अनुप्रयोगों के बारे में पढेग़े।
वास्तविक विलयन, कोलाइडी विलयन और निलंबन के बीच भिन्नता
आप जानते है। कि पानी में शर्करा का विलयन समागं होता है, पर दूध में नहीं। दूध को ध्यान से देखने पर उसमें तेल की बूंदें तैरती दिखेगी। इसलिए, यघपि वह समांग लगता है पर वास्तव में वह विशमांग होता है। सभी प्रकार के विलयनों का स्वभाव विलेय कणों के आमाप पर निर्भर करता है। यदि आमाप 1 से 100 nm के बीच हो तो कोलाइडी विलयन बनता है, जब विलेय कणों का आमाप 100 nm से अधिक हो तो वह निलंबन के रूप में पाया जाता है। इस प्रकार कोलाइडी विलयन वास्तविक विलयन और निलंबन के बीच की अवस्था होती है।कोलाइडी विलयन की प्रावस्थाएँ
कोलाइडी विलयन विशमांग होते हैं और उनमें कम से कम दो प्रावस्थाएँ होती हैं परिक्षिप्त प्रावस्था और परिक्षेपण माध्यम।1. परिक्षिप्त प्रावस्था: वह पदार्थ जो कम मात्रा में विघमान रहता है और इसके कण
कोलाइडी आमाप (1 से 100 nm) के होते हैं।
2. परिक्षेपण माध्यम: यह वह माध्यम है जिसमें कोलाइडी कण परिक्षिप्त रहते है।
पानी में, गंधक कोलाइडी विलयन में गंधक कण परिक्षिप्त प्रावस्था बनाते हैं और पानी
परिक्षेपण माध्यम होता है।
ये दो प्रावस्थाएँ : परिक्षिप्त प्रावस्था और परिक्षेपण माध्यम, ठोस, द्रव अथवा गैस हो सकते हैं। इस प्रकार दो प्रावस्थाओं की भौतिक अवस्था के अनुसार कोलाइडी विलयन विभिन्न प्रकार के हो सकते हैं। सारणी में विभिन्न प्रकार के कोलाइडी विलयन और उनके उदाहरण दिए गए हैं।
ऊपर दिए गए विभिन्न प्रकार के कोलाइडी विलयनों में विलय (द्रव में ठोस), जैल (ठोस में जल), और पायस (द्रव में द्रव) प्रमुख है। उल्लेखनीय है कि यदि परिक्षेपण माध् यम जल हो तो विलेय को जल विलेय कहते हैं और यदि परिक्षेपण माध्यम ऐल्कोहॉल हो तो विलेय को ऐल्को विलेय कहते है।
कोलाइडी विलयनों का वर्गीकरण
कोलॉइडों विलयनों का विभिन्न प्रकार से वर्गीकरण किया जा सकता है-- प्रावस्थाओं के बीच अन्योन्य क्रिया के आधार पर
- आण्विक आमाप के आधार पर
- द्रवरागी कोलॉइड - द्रवरागी शब्द का अर्थ है विलायक के प्रति बंधुता। गोंद, जिलेटिन, स्टार्च आदि पदार्थो को जब उचित विलायक के साथ मिलाया जाता है तो वे सीधे कोलाइडी अवस्था में परिवर्तित होकर कोलाइडी विलयन बना लेते है। इस प्रकार प्राप्त विलयों को द्रवरागी विलय कहते है। इन विलयों का एक महत्वपूर्ण लक्षण यह है कि यदि परिक्षिप्त प्रावस्था को परिक्षेपण माध्यम से पृथक कर दिया जाए तो उसमे परिक्षेपण माध्यम पुन: मिलाकर विलय को दुबारा बनाया जा सकता है, यही कारण है कि इन विलयों को उत्क्रमणीय विलय कहते है। ये विलय पर्याप्त स्थाई होते है।
- द्रवविरागी कोलॉइड - द्रव विरागी शब्द का अर्थ है-विलायक के प्रति कम बंधुता ह और न जैसी धातुओं, उनके हाइड्रोक्साइडों अथवा सल्फाइडों आदि को जब परिक्षेपण माध्यम में मिलाया जाता है तो वे सीधे कोलाइडी अवस्था में परिवर्तित नहीं होते हैं। उन्हें विशेष विधियों द्वारा बनाया जाता है। ये विलय शीघ्र अवक्षेपित हो जाते हैं और इस प्रकार बहुत स्थाई नहीं होते हैं। उन्हें कोलाइडी रूप में बने रहने के लिए स्थायीकारक की आवश्यकता होती है। ये अनुत्क्रमणीय विलय होते हैं, क्योंकि अवक्षेपित होने पर ये विलायक के साथ मिलकर कोलाइडी विलयन नहीं बनाते हैं। यदि परिक्षेपण माध्यम पानी हो तो उसे जलविरागी कोलॉइड कहते हैं।
- बृहदाणुक कोलॉइड : इस प्रकार के कोलॉइड में परिक्षिप्त प्रावस्था के कणों का आमाप कोलॉइड कणों के आमाप के बराबर बड़ा होता है। (यानि 100 nm) प्रकृतिक वृहदाणुक कोलॉइडों के उदाहरण हैं : स्टार्च, सेल्यूलोस, प्रोटीन आदि।
- बहु अणुक कोलॉइड : इसमें प्रत्येक परमाणु कोलॉइड के आमाप का नहीं होता पर वे आपस में पुंज बनाकर (जुड़कर) कोलॉइड़ो के नाप के अणु बनाते है। उदाहरणार्थ : सल्फर विलय में अणुओं के पुंज कोलॉइडों के नाप के होते हैं।
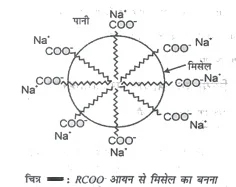
- संघटित कोलॉइड : ये पदार्थ कम सांद्रण में सामान्य विघुत अपघट्यों की तरह कार्य करते है, परन्तु अधिक सांद्रण में संघटित होकर मिसेल बनाते हैं जो कि कोलॉइड विलयन की तरह कार्य करते है। साबुन इसका उदाहरण है। साबुन लम्बी श्रृंखला वाले वसीय अम्ल R COONa का सोडियम लवण है। पानी में डालने पर साबुन RCOO- और छंदेता है। ये RCOO- आयन मलै के कण के चारों ओर संघटित होकर मिसेल बनाते है, इसे चित्र में दिखया गया है।
कोलाइडी विलयनों का विरचन
जैसा पहले बताया जा चुका है द्रवरागी विलय बनाने के लिए पदार्थो को सीधे परिक्षेपण माध्यम के साथ मिलाया जाता है। उदाहरण के लिए स्टार्च, जिलेटिन, गोंद आदि के कोलाइडी विलयन बनाने के लिए उन्हें केवल गर्म पानी पें घोला जाता है। उसी प्रकार सेलूलोस नाइट्रेट का कोलाइडी विलय बनाने के लिए उसे ऐल्कोहॉल में घोला जाता है। प्राप्त विलयन को कोलोडियन कहते है। किन्तु द्रवविरागी कोलॉइडों को प्रत्यक्ष विधि द्वारा नहीं बनाया जा सकता है। उसे बनाने के लिए दो प्रकार की विधियाँ काम में लाई जाती हैं। ये है: -- भौतिक विधि
- रासायनिक विधि
पेप्टाइजीकरण: ताजा बने अवक्षेप में उपयुक्त विघुत अपघट्य मिला कर उसे कोलॉइड में बदलने के प्रक्रम को पेप्टाइजीकरण कहते है। उदाहरणार्थ, फेरिक हाइड्रॉक्साइड के अवक्षेप में फेरिक क्लोरॉइड मिलाने पर फेरिक हाइड्रॉक्साइड भूरे लाल रंग की कोलाइडी विलयन में बदल जाता है। ऐसा अवक्षेप द्वारा विद्युत अपघ्य के धनायन के अधिशोषण के कारण होता है। Fe(OH)3 में FeCl3 डालने पर, Fe(OH)3 के कण FeCl3 के Fe3+ आयनों को अवशोषित कर लेते हैं। अत: Fe(OH)3 के कण धनावेशित हो जाते हैं और वे एक दूसरे को प्रतिकर्षित करके कोलाइडी विलयन बनाते हैं।
2. रासायनिक विधि : आक्सीकरण द्वारा - गंधक विलय प्राप्त करने के लिए H2S गैस का HNO3 अथवा Br2 जल आदि ऑक्सीकारक विलयन में बुदबुदन किया जाता है। अभिक्रिया इस प्रकार होगी :
Br2 + H2S
_
S+2HBr 2 HNO3 + H2S
2 H2O + 2NO2 + S
रासायनिक विधि द्वारा Fe(OH)3 विलय, As2S3 विलय भी बनाए जा सकते हैं।
कोलाइडी विलयनों का शोधन
जब कोलाइडी विलयन बनाया जाता है तो बहुधा उसमें विघुत अपघट्य अपद्रव्य के रूप में मौजूद रहता है, जो उसे अस्थायीकृत कर देता है। अत: कोलाइडी विलयन के शोधन के लिए निम्नलिखित विधियों का उपयोग किया जाता है:-- अपोहन (Dialysis)
- विघुत अपोहन (Electric Dialysis)
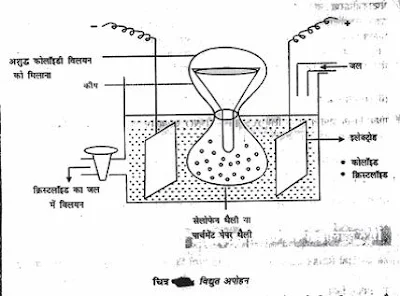
2. विघुत अपोहन -
अपोहन प्रक्रम में विघुत के उपयोग से प्रक्रम की दर बढ़ाई जा सकती
है। जब इलेक्ट्रोड़ों में विघुत प्रवाह की जाती है तो अपद्रव्य के आयन विपरीत आवेश वाले
इलेक्ट्रोड की ओर तीव्र गति से विसरित होते है। विघुत प्रवाह की उपस्थिति में किए गए
अपोहन को विघुत अपोहन कहते हैं।
अपोहन का सबसे महत्वपूर्ण उपयोग कृत्रिम वृक्क मशीनों में रूधिर के शोधन के
लिए किया जाता है। अपोहन झिल्ली में से आयन आदि छोटे कण निकल जाते हैं किन्तु
हिमोग्लोबिन आदि कोलाइडी आमाप के कण झिल्ली में से नहीं निकल पाते हैं।
कोलाइडी के गुण धर्म
कोलॉइडों के गुणधर्मो की नीचे चर्चा की गई है:-1. विशमांग लक्षण : कोलाइडी कण अपने ही सीमा पृष्ठों में रहते है। जो उन्हें परिक्षेपण माध्यम से पृथक करते है। इस प्रकार कोलाइडी तंत्र दो प्रावस्थाओं का विशमांग मिश्रण होता है। ये दो प्रावस्थाएँ है: (क) परिक्षिप्त प्रावस्था (ख) परिक्षेपण माध्यम
2. ब्राउनी गति : ब्राउनी गति नाम इसके आविष्कारक रॉबर्ट ब्राउन (वनस्पतिज्ञ) के कारण पड़ा। कोलाइडी कणों की सतं त और अनियमित टेढ़ी-मेढ़ी गति को ब्राउनी गति उत्पन्न होती है। विभिन्न दिशाओं से लगने वाले बल असमान होते हैं इसलिए कणों की गति टेढ़ी मेढ़ी होती है। विलायक के अणुओं की कोलाइडी कणों के साथ टक्कर से ब्राउनी गति उत्पन्न होती है।
3. टिन्डल प्रभाव : 1869 में टिन्डल ने प्रेक्षण किया कि यदि कोलाइडी विलयन में प्रकाश की तीव्र किरण पुंज प्रविष्ट की जाए तो प्रकाश-पथ प्रदीप्त हो जाता है। इस परिघटना को टिन्डल प्रभाव कहते है। यह परिघटना कोलाइडी कणों द्वारा प्रकाश के प्रकीर्णन से होती है । जब सूर्य की किरणों किसी रेखाछिद्र से अंधेरे कमरे में प्रवेश करती हैं तो यही प्रभाव दृष्टिगोचर होता है। यह हवा के धूल के कणों द्वारा प्रकाश के प्रकीर्णन से होता है।
4. वैघुत गुणधर्म : कोलाइडी विलयन के कण विघुत आवेशित होते है। सभी कणों में धन अथवा ऋण एकसमान आवेश होता है। परिक्षेपण माध्यम का समान और विपरीत आवेश होता है, इसलिए कोलाइडी कण एक दूसरे का प्रतिकर्शण करते है और एकत्र हाके र नीचे नहीं बैठते हैं। उदाहरण के लिए आसेनियस सल्फाइड विलय, स्वर्ण विलय, रजत विलय आदि में ऋण आवेशित कोलाइडी कण होते हैं जबकि फेरिक हाइड्रॉक्साइड, ऐल्युमिनियम हाइड्राक्साइड आदि में धन आवेशित कोलाइडी कण होते है। कोलाइडी कणों के आवेशित होने के अनेक कारण है।
- कोलाइडी कणों द्वारा धनायनों अथवा ऋणायनों का अधिषोषण
- मिसेल आवेशित होते हैं
- कोलॉइडों के विरचन के दौरान, मुख्यता ब्रेडिग आर्क विधि में कोलॉइड कण इलेक्ट्रॉनों को ग्रहण कर आवेशित हो जाते है। कोलाइडी कणों पर आवेश की उपस्थिति को वैघुत कण संचलन प्रक्रम द्वारा दिखाया जा सकता है। वैघुत कण संचलन प्रक्रम में कोलाइडी कण विघुत प्रवाह के प्रभाव से कैथोड अथवा एनोड की तरफ गतिशील होते हैं।
कोलाइडी विलयन के अनुप्रयोग
कोलॉइडों की हमारे जीवन में महत्वपूर्ण भूमिका है। उनके कुछ अनुप्रयोगों की यहाँ चर्चा की गई है।1. मल व्यवस्था: धूल, हवा आदि के कोलाइडी कणों में विघुत आवेश होता है। जब मल
को उच्च विभव पर रखी धातु की प्लेटों के बीच प्रवाहित किया जाता है तो कोलाइडी कण
विपरीत आवेशित इंलेक्ट्रोड की ओर जाते हैं और वहाँ अवक्षेपित हो जाता है। इससे
मल-जल का शोधन हो जाता है।
2. कुओं के पानी का शोधन: जब पंकिल जल में फिटकरी मिलाई जाती है तो
कोलॉइड के ऋणा आवेशित कण फिटकरी के AL3 आयनों द्वारा उदासीन हो जाते है।
इस प्रकार पंक कण नीचे बैठ जाते है और पानी को छान कर इस्तेमाल किया जा सकता
है।
3. धूम्र अवक्षेपण: धूम्र कण वास्तव में हवा में कार्बन के विघतु आवेशित कोलाइडी कण
होते है। इस कार्बन का अवक्षेण कॉट्रेल अवक्षेपण द्वारा किया जाता है। चिमनी से निकलने
वाले धुएँ को एक कक्ष में प्रविष्ट कराया जाता है। कक्ष में अनेक धातु प्लेटें एक धातु के
तार से जुड़ी रहती है। यह तार उच्च विभव स्त्रोत से जुडा़ रहता है । धुएँ के आवेशित कण विपरीत आवेश वाले इलेक्ट्रोड की ओर आकृष्ट
होकर अवक्षेपित हो जाते है। और गरम स्वच्छ वायु बाहर निकल जाती है।
4. फोटोग्राफी : जिलेटिन में सिल्वर ब्रोमाइड के कोलाइडी विलयन को काँच की प्लेंटो
अथवा सेलुलाइड फिल्मों पर प्रयुक्त किया जाता है। इस प्रकार फोटोग्राफी में प्रयोग
होनेवाली सुग्राही फिल्में प्राप्त होती है।
5. रूधिर आतंचन : रूधिर, कोलाइडी विलयन है जो ऋण आवेशित होता है। Fecl3 विलयन प्रयुक्त करने पर रूधिर का बहना बंद हो जाता है और रूधिर आतंचन हो जाता
है। इसका कारण यह है कि Fe3+ आयन रूधिर के कोलाइडी कणों के आवेश को उदासीन
कर देते हैं जिससे आतंचन हो जाता है।
6. रबर पट्टन : लेटेक्स, ऋण आवेशित रबर कणों का कोलाइडी विलयन होता है।
जिस वस्तु को रबर पट्टन करना हो उसे रबर पटट्न बाथ में एनोड बनाया जाता है। ऋण
आवेशित रबर कण एनोड की ओर जाते हैं और उस पर निक्षेपित हो जाते है।
7. आकाश का नीला रंग : क्या आपने कभी सोचा कि आकाश का रंग नीला क्यों
होता है। इसका कारण यह है कि आकाश में तैरने वाले कोलाइडी धूल कण नीले प्रकाश
का प्रकीर्णन करते है। जिससे आकाश का रगं नीला दिखाई देता है। यदि आकाश में
कोलॉइड कण न होते तो पूरा आकाश अंधकारपूर्ण लगता ।
पायस के अनुप्रयोग - पायस हमारे दैनिक जीवन में महत्वपूर्ण भूमिका निभाते है। कुछ
अनुप्रयोग नीचे दिए जा रहे है:
पायस और जैल
पायस वे कोलॉइड विलयन होते हैं जिनमें परिक्षिप्त प्रावस्था और परिक्षेपण माध्यम
दोनों ही दव्र होते है। दोनों द्रव एक दूसरे में अमिश्रणीय होते है, क्योंकि मिश्रणीय होने
पर वे वास्तविक विलयन बना देगे । पायस दो प्रकार के होते है:
1. पानी में तेल का पायस: यहाँ परिक्षिप्त प्रावस्था और परिक्षेपण माध्यम पानी होता
है। इसका उदाहरण दूध है। क्योकि दूध में द्रव वसा पानी में परिक्षिप्त होती है। इसका
दूसरा उदाहरण चेहरे पर लगाने वाली क्रीम है।
2. तेल में पानी : इसमें परिक्षिप्त प्रावस्था पानी और परिक्षेपण माध्यम तेल होता है।
मक्खन, कॉड लिवर तेल, कोल्ड क्रीम आदि इसके उदाहरण है।
रखने पर अमिश्रणीय होने के कारण पायस के दोनो द्रव यानि तेल और पानी
अलग हो जाते हैं। इसलिए पयास को स्थाई बनाने के लिए इसमें पायसीकरण मिलाए
जाते हैं। साबुन एक उपयोगी पायसीकरण है। पायसीकरण की उपस्थिति में पायस बनने
के प्रक्रम को पायसीकरण कहते हैं। पायसीकरण कैसे कार्य करता है? पायसीकरण तेल और पानी के अंतरापृष्ठ पर
सांद्रित होकर उन्हे बांध देता है।
- कपड़ों और शरीर पर से मैल धोने की साबुन और संश्लेशित अपमार्जक की प्रक्रिया, तेल और पानी के पायस बनने पर ही आधारित है।
- दूध, पानी और वसा का पायस हैं। मक्खन और क्रीम भी पायस है।
- विभिन्न प्रकार की चेहरे की क्रीम और लोशन भी पायस है।
- कॉड लिवर तेल जैसी तलीय औशधि जल्दी और बेहतर अवशोषण के लिए पायस के रूप में दी जाती है। कुछ मरहम भी पायसीकरण द्वारा होता है।
- आंतों में वसा का पायन भी पायसीकरण द्वारा होता है।
- सल्फाइड अयस्क के शोधन के लिए प्रयुक्त फेन प्लवन प्रक्रम में उसका तेल का पायस के साथ उपचा किया जाता है। मिश्रण को संपीडित वायु से प्रक्षेपित करने पर अयस्क कण पृष्ठ पर आ जाते हैं, तब उन्हें अलग कर लिया जाता है।
जैल दो प्रकार के होते है - लचीले जैल और अलचीले जैल।
लचीले जलै उत्क्रमणीय होते है। पानी खोने पर जैसे वे जमते है पानी मिलाने पर
वे वापिस मूल अवस्था में आ जाते है। अलचीले जैल अनुत्क्रमणीय होते है।
जैल कई प्रकार से उपयोग में आते है। सिलिका, पनीर, जैली, बूट पॉलिश, दही,
काफी उपयोग होनेवाले जैल है। ठोस एल्कोल ईधन, ऐल्कोहल का कैल्सियम एसिटेट में
जैल है।